 Антитяло-зависимата клетъчна цитотоксичност (ADCC) е основният механизъм на действие за няколко предлагани на пазара терапевтични антитела (mAbs) и за много други включени в клинични изпитвания. Ефикасността на ADCC силно зависи от способността на терапевтичните mAbs да набират ефекторни клетки като естествени клетки убийци, които индуцират апоптозата на целевите клетки. Набирането на ефекторни клетки от mAbs се влияе отрицателно от модификация на фукоза на N-гликани върху Fc; по този начин, използването на афукозилиран mAbs е тенденция за подобрена ADCC терапия. Повечето афукозилирани mAbs в клинично или търговско производство са произведени от клетки гостоприемници на клетки от яйчници на китайски хамстер (CHO), като обикновено генерират ниски добиви в сравнение с дивизионен тип гостоприемник. Изследването описва подробно създаването и характеризирането на две модифицирани CHOZN® клетъчни линии, в които ензимът, участващ в синтеза на гуанозин дифосфат (GDP) -фукоза, GDP маноза-4,6-дехидратаза (Gmds) и GDP-L-фукоза синтаза (FX) ), е елиминиран. Най-добрите клетъчни линии на гостоприемника за всеки от нокаутите, FX – / – и Gmds – / -, са избрани въз основа на устойчивостта на растежа, избирателния толеранс към количеството MSX, производствения титър, нивото на фукозилиране и клетъчната стабилност. Тествано е производството на две патентовани IgG1 mAbs в модифицирани клетки гостоприемници и е установено, че титрите са сравними с клетките CHOZN®. MAbs, генерирани от която и да е от клетъчна линия на KO, показват липса на модификация на фукоза, което води до значително подсилени FcγRIIIa и ADCC ефекти. Тези данни демонстрират, че и двата вида клетки гостоприемници FX – / – и Gmds – / – могат да заменят клетки Fut8 – / – CHO за клинично производство на терапевтични антитела. Повече информация може да получите тук.
Антитяло-зависимата клетъчна цитотоксичност (ADCC) е основният механизъм на действие за няколко предлагани на пазара терапевтични антитела (mAbs) и за много други включени в клинични изпитвания. Ефикасността на ADCC силно зависи от способността на терапевтичните mAbs да набират ефекторни клетки като естествени клетки убийци, които индуцират апоптозата на целевите клетки. Набирането на ефекторни клетки от mAbs се влияе отрицателно от модификация на фукоза на N-гликани върху Fc; по този начин, използването на афукозилиран mAbs е тенденция за подобрена ADCC терапия. Повечето афукозилирани mAbs в клинично или търговско производство са произведени от клетки гостоприемници на клетки от яйчници на китайски хамстер (CHO), като обикновено генерират ниски добиви в сравнение с дивизионен тип гостоприемник. Изследването описва подробно създаването и характеризирането на две модифицирани CHOZN® клетъчни линии, в които ензимът, участващ в синтеза на гуанозин дифосфат (GDP) -фукоза, GDP маноза-4,6-дехидратаза (Gmds) и GDP-L-фукоза синтаза (FX) ), е елиминиран. Най-добрите клетъчни линии на гостоприемника за всеки от нокаутите, FX – / – и Gmds – / -, са избрани въз основа на устойчивостта на растежа, избирателния толеранс към количеството MSX, производствения титър, нивото на фукозилиране и клетъчната стабилност. Тествано е производството на две патентовани IgG1 mAbs в модифицирани клетки гостоприемници и е установено, че титрите са сравними с клетките CHOZN®. MAbs, генерирани от която и да е от клетъчна линия на KO, показват липса на модификация на фукоза, което води до значително подсилени FcγRIIIa и ADCC ефекти. Тези данни демонстрират, че и двата вида клетки гостоприемници FX – / – и Gmds – / – могат да заменят клетки Fut8 – / – CHO за клинично производство на терапевтични антитела. Повече информация може да получите тук.
Публикации
Естествена история на множествен дефицит на сулфатаза: Ретроспективно фенотипизиране и анализ на функционални варианти за характеризиране на ултра-рядко заболяване
 Множественият дефицит на сулфатаза (MSD) е ултра-рядко невродегенеративно разстройство, причинено от патогенни варианти на SUMF1. Този ген кодира генериращ формилглицин ензим (FGE), протеин необходим за активиране на сулфатазата. Клиничният ход на MSD е резултат от адитивния ефект на всеки дефицит на сулфатаза, включително метахроматична левкодистрофия (MLD), няколко мукополизахаридози (MPS II, IIIA, IIID, IIIE, IVA, VI), хондродисплазия и X-свързана ихтиоза. Известно е, че засегнатите индивиди демонстрират сложен и тежък фенотип, връзката генотип-фенотип и подробният клиничен ход са неизвестни. Докладвано е за 35 случая, включени в ретроспективно проучване за естествената история. Неврологичната функция е оценена с ретроспективни скали. Извършено е биохимично и математическо моделиране на нови варианти на SUMF1. Генотипите са класифицирани въз основа на прогнозираната функционална промяна и на всеки индивид е поставена стойност за тежест на генотипа. Средната възраст за поява на симптома е 0,25 години; средната възраст за поставяне на диагнозата е 2,7 години; средната възраст, при която настъпва фатален изход е 13 години. При всички индивиди е наблюдавано забавяне в развитието, а само при част от тях се стига до амбулация и вербална комуникация. Всички пациенти показват системно увеличаване на тежестта на симптомите. По-ранната възраст за поява на симптомите и тежките варианти на патогенност корелира с лоши неврологични резултати. Чрез използване на ретроспективно фенотипизиране и подробен анализ на вариантите е определена естествената история на MSD. Установено е, че атенюираните случаи могат да бъдат разграничени от тежките случаи по възраст на поява, постигане на амбулация и генотип. Резултатите от проучването могат да помогнат за изготвянето на прогнозата и да улеснят бъдещия дизайн на изследването. Повече информация може да получите тук.
Множественият дефицит на сулфатаза (MSD) е ултра-рядко невродегенеративно разстройство, причинено от патогенни варианти на SUMF1. Този ген кодира генериращ формилглицин ензим (FGE), протеин необходим за активиране на сулфатазата. Клиничният ход на MSD е резултат от адитивния ефект на всеки дефицит на сулфатаза, включително метахроматична левкодистрофия (MLD), няколко мукополизахаридози (MPS II, IIIA, IIID, IIIE, IVA, VI), хондродисплазия и X-свързана ихтиоза. Известно е, че засегнатите индивиди демонстрират сложен и тежък фенотип, връзката генотип-фенотип и подробният клиничен ход са неизвестни. Докладвано е за 35 случая, включени в ретроспективно проучване за естествената история. Неврологичната функция е оценена с ретроспективни скали. Извършено е биохимично и математическо моделиране на нови варианти на SUMF1. Генотипите са класифицирани въз основа на прогнозираната функционална промяна и на всеки индивид е поставена стойност за тежест на генотипа. Средната възраст за поява на симптома е 0,25 години; средната възраст за поставяне на диагнозата е 2,7 години; средната възраст, при която настъпва фатален изход е 13 години. При всички индивиди е наблюдавано забавяне в развитието, а само при част от тях се стига до амбулация и вербална комуникация. Всички пациенти показват системно увеличаване на тежестта на симптомите. По-ранната възраст за поява на симптомите и тежките варианти на патогенност корелира с лоши неврологични резултати. Чрез използване на ретроспективно фенотипизиране и подробен анализ на вариантите е определена естествената история на MSD. Установено е, че атенюираните случаи могат да бъдат разграничени от тежките случаи по възраст на поява, постигане на амбулация и генотип. Резултатите от проучването могат да помогнат за изготвянето на прогнозата и да улеснят бъдещия дизайн на изследването. Повече информация може да получите тук.
Стандартизирани структури от данни при редки болести: CDISC Ръководства на потребителя за мускулна дистрофия на Дюшен и болест на Хънтингтън
 Интересът към разработването на лекарства за редки заболявания се е увеличил драстично след приемането на Закона за лекарствата сираци в САЩ през 1983 г., като 40% от новите одобрения за лекарства през 2019 г. са насочени към редките симптоми. Ограниченото разбиране на естествената история и прогресирането на заболяването възпрепятства напредъка и увеличава рисковете, свързани с разработването на лекарства за редки заболявания. Използването на международни стандарти може да помогне за съгласуване на данните, да позволи техния обмен и обединяване в по-големи набори от данни и разбиране на естествената история на заболяването. Американската Агенцията за контрол на храните и лекарствата (FDA) изисква използването на Консорциум за стандарти за обмен на клинични данни (CDISC) при приемане на нови лекарства, за да се помогне на агенцията ефективно да получава, обработва, рецензира и архивира подадените документи, както и да помогне за обединяването на данните, за да отговори на изследователски въпроси. Такива бази данни са в основата на усилията за откриване на биомаркери и подходящи за целта модели, одобрени от регулаторите. В обзора е описано развитието на CDISC фармако-терапевтични ръководства за мускулна дистрофия на Дюшен и болест на Хънтингтън чрез консорциумите на Critical Path Institute. Тези ръководства описват официални структури от данни и стандартизирана терминология за картографиране и обединяване на информация от различни източници. Това води до по-добра стандартизация за събирането на данни и позволява обединяване и сравняване на данни от множество проучвания. Обединяването на тези данни дава възможност за по-добро разбиране на прогресията на заболяването, което може да помогне за преодоляване на често срещаните предизвикателства при дизайн на клинични изпитвания при тези и други редки заболявания. В обобщение, стандартизацията на клиничните данни ще доведе до по-бърз път към регулаторно одобрение на спешно необходими нови терапии за пациенти. Повече информация може да получите тук.
Интересът към разработването на лекарства за редки заболявания се е увеличил драстично след приемането на Закона за лекарствата сираци в САЩ през 1983 г., като 40% от новите одобрения за лекарства през 2019 г. са насочени към редките симптоми. Ограниченото разбиране на естествената история и прогресирането на заболяването възпрепятства напредъка и увеличава рисковете, свързани с разработването на лекарства за редки заболявания. Използването на международни стандарти може да помогне за съгласуване на данните, да позволи техния обмен и обединяване в по-големи набори от данни и разбиране на естествената история на заболяването. Американската Агенцията за контрол на храните и лекарствата (FDA) изисква използването на Консорциум за стандарти за обмен на клинични данни (CDISC) при приемане на нови лекарства, за да се помогне на агенцията ефективно да получава, обработва, рецензира и архивира подадените документи, както и да помогне за обединяването на данните, за да отговори на изследователски въпроси. Такива бази данни са в основата на усилията за откриване на биомаркери и подходящи за целта модели, одобрени от регулаторите. В обзора е описано развитието на CDISC фармако-терапевтични ръководства за мускулна дистрофия на Дюшен и болест на Хънтингтън чрез консорциумите на Critical Path Institute. Тези ръководства описват официални структури от данни и стандартизирана терминология за картографиране и обединяване на информация от различни източници. Това води до по-добра стандартизация за събирането на данни и позволява обединяване и сравняване на данни от множество проучвания. Обединяването на тези данни дава възможност за по-добро разбиране на прогресията на заболяването, което може да помогне за преодоляване на често срещаните предизвикателства при дизайн на клинични изпитвания при тези и други редки заболявания. В обобщение, стандартизацията на клиничните данни ще доведе до по-бърз път към регулаторно одобрение на спешно необходими нови терапии за пациенти. Повече информация може да получите тук.
 На 3 октомври от 16:00 ч. до 19:30 ч. ще се проведе онлайн събитието на Световен алианс на организациите за заболявания на хипофизата (WAPO), в който членува Асоциация Хипофиза. Събитието ще има превод на руски и английски език. Регистрацията е безплатна. Повече информация може да получите тук.
На 3 октомври от 16:00 ч. до 19:30 ч. ще се проведе онлайн събитието на Световен алианс на организациите за заболявания на хипофизата (WAPO), в който членува Асоциация Хипофиза. Събитието ще има превод на руски и английски език. Регистрацията е безплатна. Повече информация може да получите тук.
Клинични, електрофизиологични и генетични характеристики на детските наследствени полиневропатии
 Наследствените полиневропатии са разнородна група заболявания на периферната нервна система. В това проучване са изследвани демографските, клиничните, електрофизиологичните и генетичните характеристики на пациентите с наследствена полиневропатия, диагностицирани и проследявани в клиника в Измир, Турция. Пациентите, които са диагностицирани с наследствени полиневропатии по време на изследвания на нервната проводимост в клиниката, са оценени ретроспективно. В общо 1484 проучвания на нервната проводимост 207 пациенти са диагностицирани с полиневропатия. Деветдесет и девет от тези пациенти са установени, че имат наследствена полиневропатия, 52 от които са мъже и 47 са жени. Шестдесет и девет пациенти с наследствена полиневропатия отговарят на аксонална, а 30 на демиелинизираща полиневропатия. Генетичен анализ е извършен при 69 пациенти и 49 от тях са генетично диагностицирани, което е довело до степен на диагностика от 71%. Напредъкът в генетиката е довел до увеличаване на хетерогенността на наследствените полиневропатии, което води до затруднения при използването на съществуващите класификации. Въпреки че типичните мутации, които се очакват при възникналите в детството полиневропатии, се наблюдават по-рядко, полиневропатиите често се срещат като открития на сложни, мултисистемни заболявания. Повече информация може да получите тук.
Наследствените полиневропатии са разнородна група заболявания на периферната нервна система. В това проучване са изследвани демографските, клиничните, електрофизиологичните и генетичните характеристики на пациентите с наследствена полиневропатия, диагностицирани и проследявани в клиника в Измир, Турция. Пациентите, които са диагностицирани с наследствени полиневропатии по време на изследвания на нервната проводимост в клиниката, са оценени ретроспективно. В общо 1484 проучвания на нервната проводимост 207 пациенти са диагностицирани с полиневропатия. Деветдесет и девет от тези пациенти са установени, че имат наследствена полиневропатия, 52 от които са мъже и 47 са жени. Шестдесет и девет пациенти с наследствена полиневропатия отговарят на аксонална, а 30 на демиелинизираща полиневропатия. Генетичен анализ е извършен при 69 пациенти и 49 от тях са генетично диагностицирани, което е довело до степен на диагностика от 71%. Напредъкът в генетиката е довел до увеличаване на хетерогенността на наследствените полиневропатии, което води до затруднения при използването на съществуващите класификации. Въпреки че типичните мутации, които се очакват при възникналите в детството полиневропатии, се наблюдават по-рядко, полиневропатиите често се срещат като открития на сложни, мултисистемни заболявания. Повече информация може да получите тук.
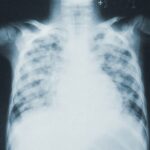 Саркоидозата е грануломатозно системно заболяване с неизвестна етиология, при което белият дроб е най-често засегнатият орган. Терапевтичното справяне със заболяването е предизвикателство, тъй като клиничното представяне и прогнозата са много разнородни. В настоящия обзор са обобщени основните постижения в терапията на саркоидозата. Текущите терапии на заболяването са категоризирани в три линии: глюкокортикоиди (първа линия), имуносупресори (втора линия) и биологични препарати (трета линия). Последните проучвания за глюкокортикоидите съобщават, че ефикасността може да бъде сходна при високи и ниски дози, но с увеличаване на страничните ефекти при по-високите дози. При имуносупресорите последните публикации, свързани с микофенолат и инжектиране на хранилище кортикотропин (RCI) добавят повече информация за тяхната употреба и ефикасност. Публикувани са нови доказателства за използването на анти–тумор некротичен фактор (анти-TNFα) при рефрактерна сърдечна саркоидоза и невросаркоидоза. Повече информация може да получите тук.
Саркоидозата е грануломатозно системно заболяване с неизвестна етиология, при което белият дроб е най-често засегнатият орган. Терапевтичното справяне със заболяването е предизвикателство, тъй като клиничното представяне и прогнозата са много разнородни. В настоящия обзор са обобщени основните постижения в терапията на саркоидозата. Текущите терапии на заболяването са категоризирани в три линии: глюкокортикоиди (първа линия), имуносупресори (втора линия) и биологични препарати (трета линия). Последните проучвания за глюкокортикоидите съобщават, че ефикасността може да бъде сходна при високи и ниски дози, но с увеличаване на страничните ефекти при по-високите дози. При имуносупресорите последните публикации, свързани с микофенолат и инжектиране на хранилище кортикотропин (RCI) добавят повече информация за тяхната употреба и ефикасност. Публикувани са нови доказателства за използването на анти–тумор некротичен фактор (анти-TNFα) при рефрактерна сърдечна саркоидоза и невросаркоидоза. Повече информация може да получите тук.
 Стремим се да допринасяме както за подобряване грижите и живота на хората с редки болести, така и за подобряване качеството на нашата работа. Каним всички участници в XI Национална конференция за редки болести и лекарства сираци да споделят впечатления, като попълнят кратка анкета. Нейната цел е да разберем гледната точка и мнение, относно проведената конференция. Благодарим предварително за съдействието!
Стремим се да допринасяме както за подобряване грижите и живота на хората с редки болести, така и за подобряване качеството на нашата работа. Каним всички участници в XI Национална конференция за редки болести и лекарства сираци да споделят впечатления, като попълнят кратка анкета. Нейната цел е да разберем гледната точка и мнение, относно проведената конференция. Благодарим предварително за съдействието!
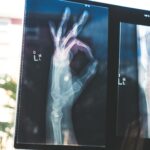 Този обзор описва нова стратегия за грижи при пациенти с остеогенезис имперфекта, базирана на работата на интердисциплинарен екип. Целта е да се осъществят три основни цели: предлагане на задълбочено координирано управление за всички и подобряване на физическата активност и качеството на живот на пациентите. При редки заболявания като остеогенезис имперфекта (ОИ) пациентите и техните семейства често страдат, поради неадекватно разпознаване на заболяването им, лоша координация на грижите и непълна информираност. Координираният интердисциплинарен подход е едно от възможните решения за предоставяне както на цялостни, така и на икономически ефективни грижи за удовлетворението на пациентите. Лошата физическа активност и нарушеното качество на живот представляват значителна тежест за тези пациенти. За справяне по-добре с тези проблеми, през 2012 г. е създаден интердисциплинарен екип за справяне с пациенти с ОИ в университетски болничен център (CHUV, Университетска болница в Лозана). Повече информация може да получите тук.
Този обзор описва нова стратегия за грижи при пациенти с остеогенезис имперфекта, базирана на работата на интердисциплинарен екип. Целта е да се осъществят три основни цели: предлагане на задълбочено координирано управление за всички и подобряване на физическата активност и качеството на живот на пациентите. При редки заболявания като остеогенезис имперфекта (ОИ) пациентите и техните семейства често страдат, поради неадекватно разпознаване на заболяването им, лоша координация на грижите и непълна информираност. Координираният интердисциплинарен подход е едно от възможните решения за предоставяне както на цялостни, така и на икономически ефективни грижи за удовлетворението на пациентите. Лошата физическа активност и нарушеното качество на живот представляват значителна тежест за тези пациенти. За справяне по-добре с тези проблеми, през 2012 г. е създаден интердисциплинарен екип за справяне с пациенти с ОИ в университетски болничен център (CHUV, Университетска болница в Лозана). Повече информация може да получите тук.
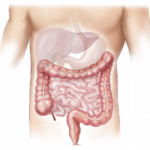 Синдромът на късото черво (СКЧ) е рядко заболяване, което е резултат от обширна резекция на червата. Когато останалата абсорбционна повърхност на червата не може да усвои достатъчно макронутриенти, микронутриенти и вода, СКЧ води до чревна недостатъчност (ЧН). Пациентите със СКЧ, които страдат от ЧН, се нуждаят от парентерално хранене за да оцелеят, но дългосрочното парентерално хранене може да доведе до усложнения като катетър-свързан сепсис и метаболитни заболявания. Спонтанната чревна адаптация се случва седмици до месеци след резекция, което води до хиперплазия на останалите черва, изменение в нивата на чревните хормони, дисбиоза и хиперфагия. Пероралното хранене и наличието на дебело черво са две основни причини за тази адаптация. Обзорът има за цел да обобщи настоящите познания за механизмите, скрити в спонтанната чревна адаптация, особено в отговор на модификации на луминалното съдържание, включително хранителните вещества. В бъдеще диетичните манипулации могат да се използват за лечение на СКЧ. Повече информация може да получите тук.
Синдромът на късото черво (СКЧ) е рядко заболяване, което е резултат от обширна резекция на червата. Когато останалата абсорбционна повърхност на червата не може да усвои достатъчно макронутриенти, микронутриенти и вода, СКЧ води до чревна недостатъчност (ЧН). Пациентите със СКЧ, които страдат от ЧН, се нуждаят от парентерално хранене за да оцелеят, но дългосрочното парентерално хранене може да доведе до усложнения като катетър-свързан сепсис и метаболитни заболявания. Спонтанната чревна адаптация се случва седмици до месеци след резекция, което води до хиперплазия на останалите черва, изменение в нивата на чревните хормони, дисбиоза и хиперфагия. Пероралното хранене и наличието на дебело черво са две основни причини за тази адаптация. Обзорът има за цел да обобщи настоящите познания за механизмите, скрити в спонтанната чревна адаптация, особено в отговор на модификации на луминалното съдържание, включително хранителните вещества. В бъдеще диетичните манипулации могат да се използват за лечение на СКЧ. Повече информация може да получите тук.

Лице за контакти:
Моника Милкова Маринова
Мобилен телефон:
0885 44 00 19
Адрес за кореспонденция:
ул. „Средна гора“ 2,
6008 Стара Загора
Електронна поща:
marinova_tarlov@abv.bg
Фейсбук група – затворена ( предназначена за пациенти) „Група Периневрални кисти на Тарлов
България“ – членството се одобрява след представен ЯМР.
Фейсбук страница на сдружението – Сдружение на Тарловите пациенти в България- Лечение без
граници
Управителен съвет:
Моника Милкова Маринова – председател
Женя Ангелова Стоенчева – член на УС
Росица Минчева Минчева-Нанева – член на УС
Сдружението има за цел:
Защита на правата на хората с редки болести, включително страдащите от Периневрални кисти на Тарлов;
Подпомагане, обединяване, насърчаване и информиране на хора с Периневрални кисти на Тарлов и адаптирането им към обществото;
Подпомагане на професионалното развитие и квалификация на изследователите и медиците в областта, свързана с профилактиката, диагностиката, лечението и рехабилитацията на Периневрални кисти на Тарлов;
Запознаване на обществото с особеностите на заболяването, профилактиката, диагностиката, лечението и рехабилитацията на Периневрални кисти на Тарлов, с физиологическите и психологическите последствия от него;
Насърчаване, подпомагане и развитие на изследвания за Периневрални кисти на Тарлов в чужбина;
Създаване на контакти с подобни организации в чужбина;
Осъществяване на контакти и постоянен диалог между сдружението и органите и организациите в регионален и световен мащаб, имащи отношение към редките болести, включително и Периневрални кисти на Тарлов;
Предприемане на мерки за преодоляване на емоционалните последствия от болестите;
Професионална преквалификация и социална рехабилитация на хората с редки болести, включително страдащите от Периневрални кисти на Тарлов;
Осигуряване на средства за лечение и подпомагане на болните от Периневрални кисти на Тарлов.
