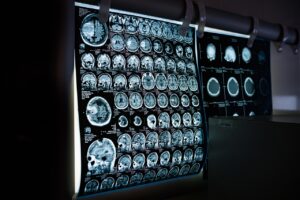
 Саркоидозата се дефинира като имуномедиирано мултиорганно грануломатозно заболяване с неизвестна етиология, което се характеризира с наличието на множество неказеозни грануломи при липса на определена инфекциозна или токсична причина. Невросаркоидоза (НС) възниква, когато саркоидните грануломи засягат централната или периферната нервна система. Саркоидозата обикновено се проявява с неспецифични прояви, включително суха кашлица, умора, нощно изпотяване, загуба на тегло, кожни промени и очни прояви. Много пациенти, които развиват НС, имат неврологични прояви в рамките на две години след диагностицирането на саркоидоза. В тази статия се представя случай на новодиагностицирана саркоидоза при 49-годишен пациент от мъжки пол, първоначално с неврологични прояви с неизвестен произход, по-късно идентифицирани като НС при биопсия на периферни лимфни възли с неказеозиращ гранулом. Прочетете цялата статия тук.
Саркоидозата се дефинира като имуномедиирано мултиорганно грануломатозно заболяване с неизвестна етиология, което се характеризира с наличието на множество неказеозни грануломи при липса на определена инфекциозна или токсична причина. Невросаркоидоза (НС) възниква, когато саркоидните грануломи засягат централната или периферната нервна система. Саркоидозата обикновено се проявява с неспецифични прояви, включително суха кашлица, умора, нощно изпотяване, загуба на тегло, кожни промени и очни прояви. Много пациенти, които развиват НС, имат неврологични прояви в рамките на две години след диагностицирането на саркоидоза. В тази статия се представя случай на новодиагностицирана саркоидоза при 49-годишен пациент от мъжки пол, първоначално с неврологични прояви с неизвестен произход, по-късно идентифицирани като НС при биопсия на периферни лимфни възли с неказеозиращ гранулом. Прочетете цялата статия тук.
Публикации
 Регистрите за редки болести (РРБ) улесняват наблюдението на редките болести чрез обединяване на малки набори от данни, за да се повишат клиничните и епидемиологични познания за редките болести и да се насърчат най-добрите практики, ориентирани към пациента. Целта на това проучване е да разбере текущото състояние на РРБ в Австралия, събраните данни, въздействието върху резултатите на пациентите, моделите на финансиране и бариерите и факторите, които позволяват тяхното създаване и поддържане.
Регистрите за редки болести (РРБ) улесняват наблюдението на редките болести чрез обединяване на малки набори от данни, за да се повишат клиничните и епидемиологични познания за редките болести и да се насърчат най-добрите практики, ориентирани към пациента. Целта на това проучване е да разбере текущото състояние на РРБ в Австралия, събраните данни, въздействието върху резултатите на пациентите, моделите на финансиране и бариерите и факторите, които позволяват тяхното създаване и поддържане.
Четиридесет РРБ отговарят на проучването; девет са национални, пет са базирани в Австралия и Нова Зеландия, а останалите са глобални. От 40 респонденти на проучването осем са интервюирани. Основните предизвикателства се оказват разходите/финансирането на събирането на данни, пълнотата на данните и съгласието на пациента. Когато са попитани, участниците идентифицираха възможности и предизвикателства по отношение на потенциалните опции за рационализиране на РРБ в Австралия в бъдеще.
Констатациите от това проучване подчертават значителна хетерогенност на набора от данни въз основа на отделното заболяване и настоящата липса на оперативна съвместимост и координация между различните РРБ в Австралия. Независимо от това следва да се проучи национално координиран подход към РРБ, като се имат предвид конкретните ползи, които РРБ предлагат, като достъп до изследвания и наблюдение на нови лечения, повлияващи заболяването. Прочетете цялата статия тук.
Ролята на пациентските организации в научноизследователската и развойна дейност: Доказателства за редки болести
 Пациентските организации играят все по-важна роля във фармацевтичния сектор, но тяхното въздействие върху иновациите остава неизследвано. В тази статия се оценява въздействието на пациентските организации върху научноизследователската и развойната дейност в контекста на редките заболявания в Европа, като се използва собствен набор от данни, който картографира клиничните изпитвания от откриването до фаза III в 29 държави, 1893 показания и 30 години (1990-2019). Чрез прилагане на методологии за разлики в събитията към панел от 1 646 910 уникални наблюдения за научноизследователската и развойна дейност (НИРД) е установено, че държава с поне една действаща пациентска организация имат по-висок процент на НИРД дейност в сравнение с тези без, с по-силен ефект в по-разпространени редки заболявания в сравнение с изключително редки състояния.
Пациентските организации играят все по-важна роля във фармацевтичния сектор, но тяхното въздействие върху иновациите остава неизследвано. В тази статия се оценява въздействието на пациентските организации върху научноизследователската и развойната дейност в контекста на редките заболявания в Европа, като се използва собствен набор от данни, който картографира клиничните изпитвания от откриването до фаза III в 29 държави, 1893 показания и 30 години (1990-2019). Чрез прилагане на методологии за разлики в събитията към панел от 1 646 910 уникални наблюдения за научноизследователската и развойна дейност (НИРД) е установено, че държава с поне една действаща пациентска организация имат по-висок процент на НИРД дейност в сравнение с тези без, с по-силен ефект в по-разпространени редки заболявания в сравнение с изключително редки състояния.
Тази статия предполага, че пациентските организации играят важна роля в насочването на усилията за НИРД в областта на редките заболявания. Необходими са допълнителни изследвания, за да се разберат по-добре механизмите, водещи до този ефект и потенциалното въздействие на пациентските организации върху съществуващите неравенства в здравеопазването. Прочетете цялата статия тук.
Използване на ORPHA кодове за кодиране на редки болести: сравнение на точността и сравнимостта между страните
 Оценката за въздействието на редките болести (РБ) върху населението по отношение на броя на засегнатите пациенти и точната дефиниция на заболяването са възпрепятствани от недостатъчното им представяне в настоящите системи за кодиране. Това проучване изучава използването на специфична система за кодифициране на РБ (ORPHA кодове) в пет европейски държави/региона (Чехия, Малта, Румъния, Испания, регион Венето-Италия) при различни източници на данни през периода януари 2019 г. – септември 2021 г.
Оценката за въздействието на редките болести (РБ) върху населението по отношение на броя на засегнатите пациенти и точната дефиниция на заболяването са възпрепятствани от недостатъчното им представяне в настоящите системи за кодиране. Това проучване изучава използването на специфична система за кодифициране на РБ (ORPHA кодове) в пет европейски държави/региона (Чехия, Малта, Румъния, Испания, регион Венето-Италия) при различни източници на данни през периода януари 2019 г. – септември 2021 г.
3133 ORPHA кода се използват за кодиране на РБ, съответстващи основно на заболяването/подтипа от класификацията на Orphanet (82,2%). Повече от половината ORPHA кодове (53,6%) описват нозологична единица с много ниско болестнос (< 1 случай на милион) и най-често улавят редки нарушения в развитието по време на ембриогенезата (31,3%) и редки неврологични заболявания (17,6%). ORPHA кодовете описват нозологичните единици по-точно от съответните кодове по МКБ 10 в 83,4% от случаите.
Установено е, че ORPHA кодовете са многофункционални по отношение на РБ, способни да осигурят лесна употреба и сравнимост между държавите в базите данни за популациите и лечебните заведения. Необходими са бъдещи изследвания на въздействието на ORPHA кодирането по отношение на броя пациенти с РЗ с подобрено кодиране в здравните информационни системи, за да се добие информация за реалния мащаб на този проблем за общественото здраве. Прочетете цялата статия тук.
Разпространение на болестта на Гоше при 600 пациенти, засегнати от моноклонална гамапатия с неопределено значение
 Болестта на Гоше е рядко автозомно рецесивно наследствено заболяване, причинено от дефицит на лизозомния ензим киселинна β-глюкозидаза. Много пациенти изпитват критично забавяне на диагнозата до 8-10 години поради нейната рядкост и променливост в признаците и симптомите, с консултация с няколко специалисти.
Болестта на Гоше е рядко автозомно рецесивно наследствено заболяване, причинено от дефицит на лизозомния ензим киселинна β-глюкозидаза. Много пациенти изпитват критично забавяне на диагнозата до 8-10 години поради нейната рядкост и променливост в признаците и симптомите, с консултация с няколко специалисти.
Това проспективно наблюдателно проучване анализира разпространението на болестта на Гоше при 600 пациенти с моноклонална гамапатия с неопределено значение (MGUS) от януари 2018 г. до февруари 2022 г.
Клиничната хетерогенност на болестта на Гоше и честата липса на осведоменост сред лекарите водят до забавяне на диагностиката и тежки клинични прояви. Ролята на MGUS при наличието на поне един клиничен признак, като нисък брой на тромбоцитите, органомегалия, болка в костите или склонност към кървене, може да помогне при започване на скрининг на болестта на Гоше с DBS, като по този начин да намали периода между появата на симптомите и диагностицирането на това рядко заболяване. Прочетете цялата статия тук.
Генетичен скрининг на новородени и дигитални технологии: Протокол на проекта, базиран на двоен подход за съкращаване на диагностичния път на редките болести в Европа
 Тъй като 72% от редките заболявания са генетични по произход и най-вече в педиатрия, генетичният скрининг на новородени представлява диагностична възможност. Screen4Care е изследователски проект, който е резултат от съвместни усилия между Европейската комисия и Европейската федерация на фармацевтичните индустрии и асоциации. Той се фокусира върху генетичен скрининг на новородени и инструменти, базирани на изкуствен интелект, които ще бъдат приложени към голяма европейска популация от около 25 000 бебета. Стратегията за неонатален скрининг се основава на целенасочено секвениране, докато секвениране на целия геном ще бъде предложено на всички включени бебета, които може да проявят ранни симптоми, но са дали отрицателен резултат при целевия скрининг на новородени, базиран на секвениране. Ще се използва алгоритми, базирани на изкуствен интелект, за идентифициране на пациенти с помощта на електронни здравни досиета и за изграждане на база данни за „проверка на симптоми“ за пациенти и доставчици на здравни услуги. S4C проектира справедлива, етична и устойчива рамка за генетичен скрининг на новородени и нови дигитални инструменти. Прочетете цялата статия тук.
Тъй като 72% от редките заболявания са генетични по произход и най-вече в педиатрия, генетичният скрининг на новородени представлява диагностична възможност. Screen4Care е изследователски проект, който е резултат от съвместни усилия между Европейската комисия и Европейската федерация на фармацевтичните индустрии и асоциации. Той се фокусира върху генетичен скрининг на новородени и инструменти, базирани на изкуствен интелект, които ще бъдат приложени към голяма европейска популация от около 25 000 бебета. Стратегията за неонатален скрининг се основава на целенасочено секвениране, докато секвениране на целия геном ще бъде предложено на всички включени бебета, които може да проявят ранни симптоми, но са дали отрицателен резултат при целевия скрининг на новородени, базиран на секвениране. Ще се използва алгоритми, базирани на изкуствен интелект, за идентифициране на пациенти с помощта на електронни здравни досиета и за изграждане на база данни за „проверка на симптоми“ за пациенти и доставчици на здравни услуги. S4C проектира справедлива, етична и устойчива рамка за генетичен скрининг на новородени и нови дигитални инструменти. Прочетете цялата статия тук.

Разработването на лекарства за редки болести е свързано с предизвикателства, не на последно място от които е достъпът до ограничените данни, налични в момента в цялата екосистема за редки болести. Повечето фармацевтични компании, които се стремят да разработват медикаменти за лечение на редки заболявания, започват усилия за идентифициране на различни източници на данни, които биха могли да бъдат информативни по отношение на разпространението на заболяването, подбора и идентифицирането на пациенти, прогресията на заболяването. Такива данни често са трудни за намиране за масови заболявания и представляват още по-голяма трудност за редки заболявания. Бъдещето на разработването на лекарства за редки болести ще разчита на засилено споделяне на данни и сътрудничество между цялата екосистема на редките болести. Един от пътищата за постигане на този резултат е разработването на ускорител за лечение на редки заболявания и платформа за анализ на данни. Прочетете цялата статия тук.
 Автозомно-доминантната левкодистрофия (ADLD) е изключително рядко, бавно прогресиращо невродегенеративно заболяване, свързано със загуба на бяло вещество в централната нервна система (ЦНС). Няколко години след първото му клинично описание е установено, че ADLD се причинява от варианти в гена LMNB1, които предизвикват неговата свръхекспресия в мозъка на пациентите. LMNB1 кодира Ламин B1, протеин от ядрената ламина. Ламин B1 регулира много клетъчни процеси като репликация на ДНК, организация на хроматина и стареене. Функциите му обаче все още не са напълно изяснени. Независимо от това, Ламин B1 заедно с другите ламини, които съставляват ядрената ламина, има ключова роля за поддържане на ядрената структура. Тъй като ядрото е динамична система, подложена както на биохимична, така и на механична регулация, е възможно промените в неговата структурна хомеостаза да се превърнат във функционални промени. В тази светлина този преглед има за цел да опише частит от доказателствата, получени до момента относно ефектите от свръхекспресията на LMNB1 върху клетъчната морфология и функционалност. Освен това, по-нататъшното изследване на ADLD морфо-функционалните последици е от съществено значение за по-доброто разбиране на това сложно заболяване. Прочетете цялата статия тук.
Автозомно-доминантната левкодистрофия (ADLD) е изключително рядко, бавно прогресиращо невродегенеративно заболяване, свързано със загуба на бяло вещество в централната нервна система (ЦНС). Няколко години след първото му клинично описание е установено, че ADLD се причинява от варианти в гена LMNB1, които предизвикват неговата свръхекспресия в мозъка на пациентите. LMNB1 кодира Ламин B1, протеин от ядрената ламина. Ламин B1 регулира много клетъчни процеси като репликация на ДНК, организация на хроматина и стареене. Функциите му обаче все още не са напълно изяснени. Независимо от това, Ламин B1 заедно с другите ламини, които съставляват ядрената ламина, има ключова роля за поддържане на ядрената структура. Тъй като ядрото е динамична система, подложена както на биохимична, така и на механична регулация, е възможно промените в неговата структурна хомеостаза да се превърнат във функционални промени. В тази светлина този преглед има за цел да опише частит от доказателствата, получени до момента относно ефектите от свръхекспресията на LMNB1 върху клетъчната морфология и функционалност. Освен това, по-нататъшното изследване на ADLD морфо-функционалните последици е от съществено значение за по-доброто разбиране на това сложно заболяване. Прочетете цялата статия тук.
Подходи, основани на фенотипа, за подобряване приоритизирането на вариантите и диагностиката на редки заболявания
 Диагностиката на редки болести и откриването на патогенни гени са революционизирани чрез секвениране на цял екзом и геном, но идентифицирането на причинителя(ите) от милионите във всеки индивид остава предизвикателство. Използването на фенотипизиране на пациенти и референтни познания за генотип-фенотип, заедно с различни данни като честота на алелите, сегрегация и прогнозирана патогенност, се оказа ефективна стратегия за справяне с този проблем. В тази статия са прегледани многобройните инструменти, които са разработени за автоматизиране на този подход и демонстриране на силата на такъв подход при няколко хиляди диагностицирани случая от проекта 100,000 Genomes. Обсъждат се още предизвикателствата, които трябва да бъдат преодолени, за да се подобрят нивата на откриване и да се помогне на повечето пациенти, които все още остават без молекулярна диагноза след най-съвременна геномна интерпретация. Прочетете цялата статия тук.
Диагностиката на редки болести и откриването на патогенни гени са революционизирани чрез секвениране на цял екзом и геном, но идентифицирането на причинителя(ите) от милионите във всеки индивид остава предизвикателство. Използването на фенотипизиране на пациенти и референтни познания за генотип-фенотип, заедно с различни данни като честота на алелите, сегрегация и прогнозирана патогенност, се оказа ефективна стратегия за справяне с този проблем. В тази статия са прегледани многобройните инструменти, които са разработени за автоматизиране на този подход и демонстриране на силата на такъв подход при няколко хиляди диагностицирани случая от проекта 100,000 Genomes. Обсъждат се още предизвикателствата, които трябва да бъдат преодолени, за да се подобрят нивата на откриване и да се помогне на повечето пациенти, които все още остават без молекулярна диагноза след най-съвременна геномна интерпретация. Прочетете цялата статия тук.
Изключително рядък случай на едновременни (синхронни) аденокарцином и карциноид на сигмоидното дебело черво на фона на Баретов хранопровод
 Според данните на GLOBOCAN 2018 колоректалният рак представлява третото по честота онкологично заболяване в света. През 2018 г. заболеваемостта от рак на дебелото черво в световен мащаб е около 2 милиона, а броят на загиналите е близо 1 милион души. Голямата заболеваемост, в комбинация с високата смъртност и късното диагностициране на колоректалния карцином определят неговата социална значимост.
Според данните на GLOBOCAN 2018 колоректалният рак представлява третото по честота онкологично заболяване в света. През 2018 г. заболеваемостта от рак на дебелото черво в световен мащаб е около 2 милиона, а броят на загиналите е близо 1 милион души. Голямата заболеваемост, в комбинация с високата смъртност и късното диагностициране на колоректалния карцином определят неговата социална значимост.
Най-честите симптоми включват желязодефицитен тип анемия, промяна в дефекационния ритъм, редукция на тегло и прояви на чревна непроходимост. Не винаги обаче първата изява на клинична сиптоматика е от страна на дебелото черво, а и от други органи извън храносмилателната система. В тези случай ракът на дебелото черво обикновено е нелечим, вследствие развитие на екстраколонна дисеминация и развитие на съответна органна недостатъчност. Генетични фактори, заседналият начин на живот, затлъстяването, консумацията на червено месо, алкохол, тютюнопушене, някои метаболитни заболявания се считат за главни рискови фактори за възникването му.
Представяме случай на 47-годишна жена с хистологично верифицирани едновременни аденокарцином и карциноид на сигмоидното дебело черво, както и на фона на безсимптомно протичаща гастроезофагеална рефлуксна болест, усложнена с преканцерозата на хранопровода и стомаха – Баретов хранопровод. Прочетете цялата статия тук.
